Innledning
Dokumentet er ment som en støtte i prosessen med å utforme kravspesifikasjon ved anbud. Det er ikke tenkt videresendt til leverandør, men tabell 1 kan sendes som en oversikt over foretrukne desinfeksjonsmidler på anbud i Helse Midt-Norge (HMN).
Bakgrunn
Fagmiljøet i smittevern i HMN ser at det er behov for å presisere smittevernkrav ved anbud og anskaffelser. Dette for å sikre at smittevernkrav blir ivaretatt og sikre at utstyr som benyttes i pasientbehandling, pleie eller undersøkelse ikke forårsaker helsetjenesteassosierte infeksjoner (HAI) og smitteoverføring ved våre helseinstitusjoner. Fagmiljøet i smittevern har som intensjon å delta i arbeid med anbud og anskaffelser når dette er aktuelt og nødvendig, men kan også tas inn som kun høringsinstans når dette er tilstrekkelig. Fagmiljøet anbefaler at dette dokumentet gjennomgås tidlig i anbudsprosessen og benyttes ved utarbeidelse av kravspesifikasjoner til anbud og anskaffelser i HMN. Vi ser på dette dokumentet som et dynamisk dokument der forbedringer og oppdateringer fortløpende kan være nødvendig og at innholdet ikke er uttømmende.
Denne regionale faglige føringen er utarbeidet og besluttet av smittevernpersonell ved samtlige helseforetak i HMN.
Innhold
1.0 Krav i lov og forskrift
Forskrift om smittevern i helse- og omsorgstjenesten pålegger institusjoner som yter tjenester etter spesialisthelsetjenesteloven å forebygge og begrense forekomsten av infeksjoner. Forskriften gir pålegg om å ha et infeksjonskontrollprogram (IKP). IKP skal inneholde blant annet skriftlige retningslinjer for innkjøp og reprosessering (rengjøring, desinfisering, ev. sterilisering og kontroll) av medisinsk utstyr. Dette betyr at ved anskaffelser av medisinsk utstyr, skal smittevernhensyn ivaretas med tanke på forebygging av HAI. Samtlige helseforetak i HMN har et IKP.
I forskrift til arbeidsmiljøloven, forskrift om organisering, ledelse og medvirkning står det i
§ 15-1. Gjennomgående krav om bruk av personlig verneutstyr:
«Arbeidsgiver skal stille hensiktsmessig personlig verneutstyr til rådighet for arbeidstaker hvis risiko for skade på liv eller helse hos arbeidstaker ikke kan unngås ved tekniske installasjoner på arbeidsplassen, ved endringer av arbeidsmetoder eller ved endringer av arbeidsprosesser».
Dette betyr at ved anskaffelser av verneutstyr, er arbeidsgiver forpliktet til å skaffe hensiktsmessig verneutstyr for arbeidstakerne. «Arbeidsgiver skal sørge for at personlig verneutstyr som stilles til rådighet for arbeidstaker, oppfyller kravene gitt i forskrift om konstruksjon, utforming og produksjon av personlig verneutstyr (PVU), og dermed er CE-merket», jf. § 15-3.
Lov om medisinsk utstyr, LOV-2020-05-07-37, gjennomfører forordning om medisinsk utstyr (MDR) og forordning om in vitro-diagnostisk medisinsk utstyr (IVDR) i norsk rett. Forordningene gjennomføres i § 1 første ledd. Loven inneholder nødvendige fullmakter til å gi mer detaljerte bestemmelser i forskrift der forordningene åpner for dette.
Forskrift 9. mai 2021 nr. 1476 om medisinsk utstyr
Forskrift om medisinsk utstyr, hjemlet i lov om medisinsk utstyr, inneholder utfyllende nasjonale bestemmelser om blant annet ansvarlig myndighet, språkkrav og bruk av medisinsk utstyr. Forskriften inneholder i tillegg presisering av enkelte overgangsbestemmelser.
Forordning (EU) nr. 2017/745 om medisinsk utstyr (MDR)
Forordning (EU) nr. 2017/746 om in vitro- diagnostisk medisinsk utstyr (IVDR)
Kommentar om bruk av lovverk
Innholdet i dette dokumentet er ment som generell informasjon. Det gis ingen garanti for at tolkningen av gjeldende regelverk er fullstendig eller korrekt.
Brukere av dokumentet er selv ansvarlige for å kontrollere gjeldende lovtekst og sikre korrekt tolkning basert på offisielle kilder, eller innhente juridisk bistand ved behov.
1.1 Rengjøring, desinfeksjon og sterilisering
Flergangsutstyr som tåler varme, skal rengjøres og desinfiseres i en vaskedekontaminator (instrumentvaskemaskin). Unntaksvis kjøpes det inn utstyr som ikke tåler varmedesinfeksjon og til dette utstyret benyttes kjemisk desinfeksjon. Det bør være tungtveiende grunner for å velge slikt utstyr dersom det finnes lignende utstyr på markedet som tåler varme. Skal utstyret benyttes invasivt, må utstyret også tåle sterilisering, eller ev. høygradig desinfeksjon.
Alle rengjørings- og desinfeksjonsmidler skal være merket og ha norskspråklig bruksanvisning/beskrivelse av tiltenkt bruk og være beregnet til bruk i helsetjenesten.
· Kjemiske desinfeksjonsmidler til bruk i helse- og sykepleie skal som hovedregel være godkjent av Direktoratet for medisinske produkter (DMP) Se oversikt over godkjente desinfeksjonsmidler og veiledning for bruk.
- Desinfeksjonsmiddel som er registrert som medisinsk utstyr, skal være CE-merket. Desinfeksjonsmidler som er CE-merket, er tillatt til bruk slik det framgår av merkingen på produktforpakningen. Dokumentasjon og samsvarserklæring må sendes med.
Det at et desinfeksjonsmiddel er godkjent som medisinsk utstyr, innebærer ikke at produktet er godkjent til bruk på medisinsk utstyr generelt.
- Desinfeksjonsmiddelet må godkjennes av produsenten av det spesifikke utstyret for at det skal kunne anvendes, altså at produsent har godkjent at utstyret tåler desinfeksjonsmiddelet. Dokumentasjon må sendes med. Rengjørings- og desinfeksjonsmidler som brukes på medisinsk utstyr skal vanligvis være CE‑merket. Hvis produsenten likevel godkjenner et bestemt middel til bruk på sitt utstyr, kan dette middelet også brukes.
- Noen desinfeksjonsmidler er godkjent som biocidprodukt i henhold til biocidforskriften, som forvaltes av Miljødirektoratet Biocider - produkter og regelverk.
· Produsent må dokumentere at utstyret tåler rengjøring og desinfeksjon ut fra utstyrets anvendelsesområde (f.eks. frekvens og hyppighet av dekontaminering). Det vil si at utstyr og følgeutstyr ikke forringes/skades eller at utstyrets kapasitet/ytelse ikke påvirkes i hele utstyrets levetid.
- Desinfeksjonsmidler som er definert som biocider og/eller godkjent av DMP til bruk på generelle overflater innen helsesektoren kan også benyttes til ikke-invasivt utstyr.
- Anbefalte desinfeksjonsmidler til bruk ved sykehusene i HMN, er de midler som til enhver tid er på anbud. Utstyret skal tåle minst ett av de angitte desinfeksjonsmidlene i tabell 1, i tillegg til desinfeksjonssprit.
Tabell 1 Oversikt over desinfeksjonsmidler på anbud i HMN. Oppdatert februar 2026.
|
Desinfeksjonsmidler |
Sikkerhetsdatablad |
Kommentar |
|
Antibac overflatedesinfeksjonskluter (alkohol) |
Antibac® Overflatedesinfeksjon 75% - Overflatedesinfeksjon - Kiilto Norway |
|
|
Certus overflatedesinfeksjon 85% (alkohol) |
||
|
LifeClean (klordioksid) |
|
|
|
PeraSafe (pereddiksyre) |
||
|
Saniswiss desinfeksjonskluter (hydrogenperoksid/pereddiksyre) |
||
|
Virkon (pentakalium bis(peroksymonosulfat) bis(sulfat)) |
VirKon & PeraSafe - Dokumenter - Brage Medical
|
Forslag til tekst om desinfeksjonsmidler som kan benyttes ved kravspesifikasjon ved anbud
Dersom produsenten ikke kan anbefale noen av de angitte desinfeksjonsmidlene i tabell 1, ev. i tillegg til desinfeksjonssprit, må produsenten oppgi anbefalt desinfeksjonsmiddel og legge ved dokumentasjon på at desinfeksjonsmidlet er godkjent til bruk på aktuelt utstyr (se punkt 1.1.) og er et biocid og/eller er CE-merket som medisinsk utstyr eller godkjent av DMP. Produsentens anbefalte desinfeksjonsmiddel bør faglig vurderes før bruk. Nasjonalt kvalitets- og kompetansenettverk for dekontaminering (NKKD) kan kontaktes for rådgivning. Dokumentasjon på faglig vurdering av aktuelt desinfeksjonsmiddel skal legges ved svar på konkurransen.
Byggveileder for smittevern er utarbeidet av Sykehusbygg HF i samarbeid med smittevernpersonell i Norge. Denne bør benyttes før utarbeidelse av kravspesifikasjon til anskaffelser og anbud på f.eks. system eller fasiliteter for håndhygiene, håndvasker, toaletter, dusjhoder, vannsystem, isbitmaskin, forheng, inventar og ved ombygging/nybygg.
Folkehelseinstituttet (FHI), i samarbeid med Helsedirektoratet, har ansvar for å utarbeide faglige, kunnskapsbaserte anbefalinger og håndbøker i smittevern. Det skal være særlig tungtveiende grunner for ikke å følge råd fra FHI. Faglige anbefalinger og håndbøker kan ligge til grunn ved anbud innen håndhygiene og andre hygieneprodukter, urinkateterutstyr, verneutstyr, inventar med mer. Disse ligger tilgjengelig på FHI sine sider, se her.
Standard Norge utvikler standarder blant annet for helsetjenesten. Hensikten med å bruke standarder er å bidra til økt kvalitet, pasientsikkerhet og mer effektiv bruk av fellesskapets midler. I smittevern benyttes standarder som grunnlag for krav ved anskaffelser av medisinsk utstyr, maskiner og engangs- og flergangsprodukter. Gjeldende standarder skal fremskaffes og gjøres tilgjengelig for smittevern av den som har ansvar for anskaffelsen eller anbudet dersom standard foreligger.
2.0 Smittevernkrav
Alt medisinsk utstyr som anskaffes til bruk i sykehus skal være beregnet til dette formålet, dvs. ikke være beregnet til hjemmebruk.
2.1 Utstyr i pasientomgivelser
· Alt utstyr i pasientomgivelser som ikke er i direkte kontakt med pasienten, men berøres av personalets hender under prosedyre eller behandling, må tåle rengjøring og desinfeksjon. Produsenten skal garantere at utstyr, overflater, betjeningspanel, kontaktflater o.l. på maskiner/utstyr som tastatur, mus osv. tåler manuell rengjøring og desinfeksjon med rengjørings- og desinfeksjonsmidler som produsenten anbefaler, fortrinnsvis midler som er på anbud i HMN, jf. tabell 1.
· Utstyret bør være utformet med glatte overflater, og med minst mulig strukturer og brutte flater for å optimalisere rengjørings- og desinfeksjonsprosessen.
· Produsentens anbefalte CE-merkede rengjøringsmidler til bruk i helsetjenesten skal oppgis.
· Skriftlig fremgangsmåte for rengjøring og desinfeksjon skal legges ved og være norskspråklig. Jf. forskrift om medisinsk utstyr, §6 og MDR - Vedlegg 1 - Kapittel III. Punkt 23.4 Informasjon i bruksanvisningen.
· Opplæring i rengjøring og desinfeksjon av utstyret, samt bruk/skifte av tilhørende forbruksmateriell gis om det er relevant og nødvendig for sikker og trygg bruk. Jf. MDR-Vedlegg I - Generelle krav til sikkerhet og ytelse - Kapittel I - Generelle krav. Punkt 4c.
· Det skal foreligge forslag til avtaler for service og vedlikehold for å sikre at utstyret fungerer etter hensikten og at pasientsikkerheten blir ivaretatt.
· Utstyr og maskiner skal være ferdig validert, testet og godkjent før de tas i bruk dersom dette er aktuelt. Dokumentasjon på validering, testing og godkjenning skal oppbevares i avdelingen der utstyr/maskiner brukes.
2.2 Utstyr som er i kontakt med hel hud
· Alt utstyr som er i kontakt med hel hud og inngår i pasientprosedyrer, må tåle rengjøring og desinfeksjon. Leverandøren skal garantere at utstyret tåler manuell rengjøring samt desinfeksjon med rengjørings- og desinfeksjonsmidler som leverandøren anbefaler, fortrinnsvis midler som er på anbud i HMN, jf. tabell 1. Eksempler på utstyr kan være blodtrykksmansjett, stetoskop, rullestol, undersøkelsesbenker mm.
· Utstyret bør være utformet med glatte overflater, og med minst mulig strukturer og brutte flater for å optimalisere rengjørings- og desinfeksjonsprosessen.
Skal-krav:
· Produsenten skal garantere at både utstyr og følgeutstyr tåler manuell rengjøring og desinfeksjon. Dette betyr at verken materialer, funksjon eller ytelse skal påvirkes i hele utstyrets levetid ved bruk av de desinfeksjonsmidlene leverandøren anbefaler, fortrinnsvis desinfeksjonsmidler som er på anbud i HMN, jf. tabell 1.
· Produsentens anbefalte CE-merkede rengjøringsmidler til bruk i helsetjenesten skal oppgis.
· Det skal oppgis anbefalt makstemperatur ved varmedesinfeksjon og om hele eller deler av utstyret tåler varmedesinfeksjon.
· Skriftlig fremgangsmåte for rengjøring og desinfeksjon skal legges ved og være norskspråklig. Jf. forskrift om medisinsk utstyr, §6 og MDR - Vedlegg 1 - Kapittel III. Punkt 23.4 Informasjon i bruksanvisningen.
· Opplæring i rengjøring og desinfeksjon av utstyret, samt bruk/skifte av tilhørende forbruksmateriell gis om det er relevant og nødvendig for sikker og trygg bruk. Jf. MDR-Vedlegg I - Generelle krav til sikkerhet og ytelse - Kapittel I - Generelle krav. Punkt 4c.
· Det skal foreligge forslag til avtale for service, vedlikehold og ev. validering for å sikre at utstyret fungerer etter hensikten og slik at pasientsikkerheten blir ivaretatt.
· Utstyr og maskiner skal være ferdig validert, testet og godkjent før de tas i bruk dersom dette er aktuelt. Dokumentasjon på validering, testing og godkjenning skal oppbevares i avdelingen der utstyr/maskiner brukes.
Bør-krav:
· Beskrivelse av ev. maskinell rengjøring og desinfeksjonsmetode for ev. tilleggsutstyr bør vedlegges. F.eks. pute til rullestol.
· Rengjøring og desinfeksjon bør kunne gjennomføres enkelt uten at dette er til særlig hinder for drift eller produksjon. Beskriv metode og tidsbruk. Maskinell rengjøring og varmedesinfeksjon er foretrukket som metode og vektlegges.
2.3 Utstyr som er i kontakt med slimhinner/invasivt utstyr
· Det stilles strenge krav til rengjøring, desinfeksjon og sterilisering av invasivt utstyr. Eksempler på slik utstyr kan være endoskop, kirurgiske operasjonsinstrumenter, tuber, anestesiutstyr mm.
· Invasivt utstyr (ethvert utstyr som helt eller delvis føres inn i kroppen, enten gjennom en kroppsåpning eller gjennom kroppens overflate) deles inn i:
o Semikritisk utstyr (utstyr som kommer i kontakt med slimhinner, men uten å penetrere disse) skal tåle høygradig desinfeksjon med maksimal antibakteriell effekt og fortrinnsvis tåle sterilisering. Ev. steriliseringsmetode skal oppgis og desinfeksjonsprosessen skal være validert.
o Kritisk utstyr (utstyr som kommer i direkte kontakt med blodbanen eller vev som normalt er sterilt, eller som gjennomstrømmes av væsker eller gass som tilføres sterile områder) skal tåle sterilisering. Anbefalt steriliseringsmetode skal oppgis.
Skal-krav:
· Produsenten skal garantere at både utstyr og følgeutstyr tåler manuell rengjøring og desinfeksjon. Dette betyr at verken materialer, funksjon eller ytelse skal påvirkes i hele utstyrets levetid ved bruk av de desinfeksjonsmidlene leverandøren anbefaler, fortrinnsvis desinfeksjonsmidler som er på anbud i HMN, jf. tabell 1.
· Produsentens anbefalte CE-merkede rengjøringsmidler til bruk i helsetjenesten skal oppgis.
· Desinfeksjonsmetode skal være med maksimal antibakteriell effekt, det vil si fortrinnsvis desinfeksjon i en vaskedekontaminator (instrumentvaskemaskin). Ved manuell desinfeksjon skal desinfeksjonsmidler være godkjent for kjemisk desinfeksjon med maksimal antibakteriell effekt (høygradig desinfeksjon). Det skal oppgis om hele eller deler av utstyret tåler varmedesinfeksjon. Anbefalt makstemperatur ved varmedesinfeksjon skal oppgis.
· Skriftlig fremgangsmåte for rengjøring og desinfeksjon skal legges ved og være norskspråklig. Jf. forskrift om medisinsk utstyr, §6 og MDR - Vedlegg 1 - Kapittel III. Punkt 23.4 Informasjon i bruksanvisningen.
·
Utstyret må kunne rengjøres, desinfiseres og steriliseres i
henhold til bruksanvisning uten risiko for at utstyret skades eller at
funksjonen nedsettes.
· Opplæring i rengjøring og desinfeksjon av utstyret, samt bruk/skifte av tilhørende forbruksmateriell gis om det er relevant og nødvendig for sikker og trygg bruk. Jf. MDR-Vedlegg I - Generelle krav til sikkerhet og ytelse - Kapittel I - Generelle krav. Punkt 4c.
· Det skal foreligge forslag til avtaler for service og vedlikehold for å sikre at utstyret fungerer etter hensikten og slik at pasientsikkerheten blir ivaretatt.
· Utstyr og maskiner skal være ferdig validert, testet og godkjent før de tas i bruk dersom dette er aktuelt. Dokumentasjon på validering, testing og godkjenning skal oppbevares i avdelingen der utstyr/maskiner brukes.
Bør-krav:
· Beskrivelse for ev. maskinell rengjørings-, desinfeksjons- og steriliseringsmetode bør legges ved.
· Rengjøring, desinfeksjon og sterilisering bør kunne gjennomføres enkelt uten at dette er til særlig hinder for drift eller produksjon. Beskriv metode og tidsbruk. Maskinell rengjøring og desinfeksjon er foretrukket som metode og vektlegges.
2.4 Sterilt medisinsk engangsutstyr
Sterilt medisinsk engangsutstyr er ment å brukes kun en gang under en prosedyre. Eksempler på dette kan være PVK, bandasjemateriell, ulike nåler, kompresser, blærekateter osv.
Vær oppmerksom på nærmest identisk utstyr kan leveres:
- både som engangs- og flergangsutstyr (f.eks. sakser)
- som sterilt og ikke-sterilt. (f.eks. kompresser)
- for bruk flere ganger, men bare til samme pasient (f.eks. forstøver/nebulisator)
Merking av utstyret
Ved anbud og anskaffelser er det viktig å sikre at alle krav til merking på utstyr, emballasje og i bruksanvisningen er fulgt. Se MDR - Vedlegg 1 - Kapittel III Krav til informasjonen som følger med utstyret Punkt 23. Merking og bruksanvisning
Merkingen kan f.eks. vise
- om utstyret er engangs- eller flergangsutstyr
- om utstyret er sterilt og hvilken steriliseringsmetode som er brukt
- produksjonsdato/utløpsdato
- produsent
- krav til lagring av utstyret, f.eks. temperatur, fukt, lys mm
- om utstyret er CE-merket
- LOT-nummer
Produsent skal følge: NS-EN ISO 15223-1:2021 Medisinsk utstyr — Symboler til bruk med informasjon som skal leveres av produsenten — Del 1: Generelle krav.
Bruksanvisning
Bruksanvisning skal alltid følge med og være norskspråklig. Forskrift om medisinsk utstyr. §6 Merking og bruksanvisning.
Emballasje
Sterilt medisinsk engangsutstyr emballeres i tre lag slik at produktets egenskaper og renhet ikke forringes under transport og lagring. Produktforpakning, avdelingsforpakning og transportforpakning skal sikre at utstyret ikke blir påvirket av f.eks. sollys, fuktighet og temperatursvingninger. Ved anbud og anskaffelser må riktig emballering av produktet sikres. MDR -Vedlegg 1 - Kapittel I Generelle krav Punkt 7.
Produktforpakning skal sikre at utstyret er sterilt. Forpakningene skal kunne åpnes på en slik måte at produktet bevarer sin sterilitet inntil bruk.
Emballasjen bør være i et gjenvinnbart materiale.
Illustrasjon av forpakningene:
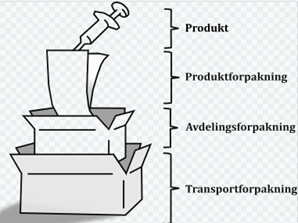
Sikker bruk
Sterilt medisinsk engangsutstyr skal designes slik at man reduserer fare for kutt og stikk ved bruk, sikrer enkel håndtering og sørger for at infeksjonsfaren ved bruk unngås eller begrenses. MDR - Vedlegg I - Kapittel II Krav til design og framstilling Punkt 11. Infeksjon og mikrobiell kontaminering.
Forslag til tekst i kravspesifikasjon ved anbud på sterilt medisinsk engangsutstyr
Sterilt medisinsk engangsutstyr skal være merket etter krav i MDR. Sterilt medisinsk engangsutstyr pakkes i tre lag emballasje og alle tre lag skal kunne avemballeres på en slik måte at produktet bevarer sin sterilitet inntil bruk. Utstyret skal utformes slik at sikker bruk ivaretas. Norskspråklig bruksanvisning skal følge med.